製薬業界におけるNRMのサービス例
Pharmacy
安全性と効率性を追求し、製薬業界の挑戦に寄り添うデジタルソリューション。情報の厳密な管理と長期保管を実現。
製薬業界では、新薬の開発等の研究開発の高コスト化や厳しい規制環境、グローバルな市場競争が激化しています。研究開発の効率化やグローバルな視野に基づいた市場戦略の構築や経営の取り組みが求められます。
製薬業界では広範な情報資産が扱われる一方で、規制や法律の厳格さのために、情報管理には厳格な対応が求められます。
また、情報の保管期間も長く、特許や競合に関しても十分な注意が必要です。

製薬業界でよくある課題
- 必要な時に文書や資料が確認できない
- 担当者の属人化により情報共有できていない
- 保存期限が正確に把握しきれていない
- 過去の文書や資料の紛失や漏洩が判別できない
- ペーパーレス化がうまくいかず文書保管のスペースが確保できない
- 最新版管理ができていないため、旧版を使い業務に支障が出ている

このような課題をお持ちであれば、NRMへ一度ご相談ください。
情報資産管理のプロフェッショナルがお客様の課題を解決いたします。
情報化戦略の力で、情報共有のスピードを加速し、製薬の未来を切り拓く。
情報資産管理で課題解決に導きます。
また、専任スタッフの派遣も行っており、導入から運用支援まで情報資産管理を中心にトータルにサポートします。お客様の現状を把握し、適切なツールの導入もご提案します。お気軽にご相談ください。
製薬業界の主なソリューション例
ドキュメント管理システムの導入
デジタル化された文書や資料を適切に管理し、必要な時に迅速にアクセスできるようにします。このシステムを導入することで、情報資産の整理、検索、共有が効率化され、業務プロセスの向上やリソースの効率的な活用が実現します。
ナレッジ共有の推進
情報やノウハウを一元化し、社内での共有を促進することで、担当者の属人化を解消し、組織全体での情報共有文化を醸成します。 これにより、迅速な意思決定と業務の効率化が可能となります。組織内での連携強化と成果の最大化に寄与します。
保存期限管理システムの導入
文書や資料の正確な保存期限を管理し、必要なタイミングで適切な措置を取ることができ、増え続ける情報資産の新陳代謝が促進できます。また、書類の保管料を削減することができます。環境への負荷軽減やオフィススペースの最適化にも寄与します。
文書トレーサビリティの確保
文書の作成者や編集履歴、アクセスログ等の情報を記録し、必要な場合に追跡できる仕組みを構築します。この仕組みにより、文書の変更やアクセスに関する詳細な情報を継続的に記録し、文書の信頼性やセキュリティを強化します。
ペーパーレス化と情報資産管理の構築
デジタル化を通じてスペースの節約や文書の検索・整理の容易化を実現し、効率的な文書保管体制を確立します。ペーパーレス化により、オフィススペースを最適化し、環境にも貢献します。また、デジタル文書は、情報の迅速な取得が可能となり、業務プロセスの効率化が促進されます。
バージョン管理システムの導入
文書や資料の変更履歴を管理し、誰がどのバージョンを使用しているのかを追跡することで、業務に支障をきたす旧版の使用 を防ぎます。このシステムにより、文書や資料の変更が容易に追跡され、正確な情報を維持し、誤った情報に基づく業務ミスを回避できます。
NRMのサービスの特長
他業種の知見と製薬業界のニーズを融合させ、最適なソリューションを提供します。
-
特長
-
分析データをもとに効果的な業務改善をご提案
製薬企業様の戦略・規制環境を理解し、サードパーティーの客観的な立場からお客様のメリットを見極め、効果的な提案を行います。 -
特長
-
他業種における経験から効果的にサポート
製薬業界に特化した支援企業ではなく、他業種での経験をお客様のニーズにカスタマイズして展開することが可能です。 -
特長
-
他企業へのアウトソースと比較して総合的なメリットを創出
専門企業(CRO等)やマンパワー企業(派遣等)へのアウトソースと比較し、業務品質、継続性、ノウハウの蓄積、標準化、コスト削減等において総合的なメリットを創出することが可能です。 -
特長
-
グローバルスタンダードに基づいたご提案
グローバルスタンダード(ISO15489レコードマネジメントガイドライン)に基づいたご提案、仕組み構築と運用サービスまでのトータルなご支援が可能です。 -
特長
-
専門スタッフが運用改善の仕組みのブラッシュアップを図る
情報資産管理の資格を有し、製薬業界において経験を積んだエキスパートを配置し、継続的に運用の改善と仕組みのブラッシュアップを図ることが可能です。
NRMにおける製薬業界の強み
製品と文書の統合したライフサイクル管理で、迅速な意思決定と効率的な業務を実現
医薬品のライフサイクル管理と情報のライフサイクル管理を統合し、連携させる体制を構築します。これにより、社内での情報共有が可能となり、業務効率化を実現します。
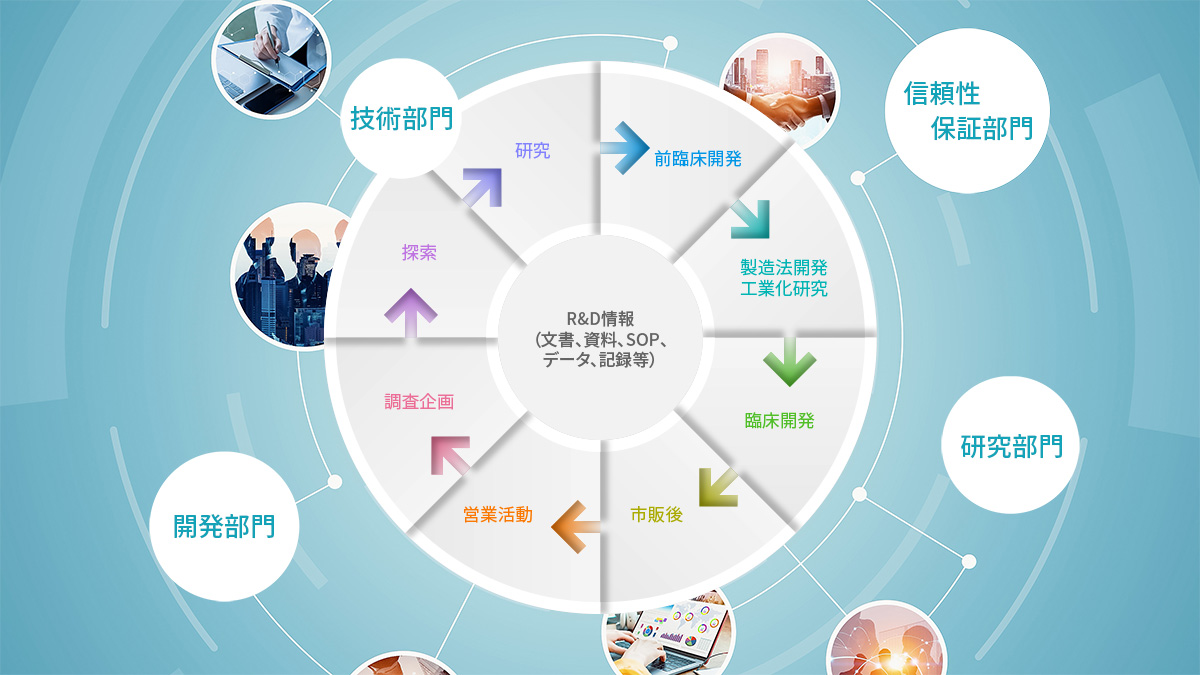
NRMを導入するメリット
-
導入メリット
-
数多くの実践経験からご提案
NRMは、その強みを長年にわたる幅広い業種・業態での経験と深い専門知識によって確立しています。独自の手法と業務分析データに基づく革新的なアプローチで、お客様の情報資産管理を効果的にサポートします。日本国内で初めてこのサービスを提供したパイオニアとして、他社にはない豊富な実績を積んでおり、安定した支援を提供することができます。 -
導入メリット
-
中立的な立場で最適なご提案
情報資産を適切に管理・活用するには、様々なツールの組み合わせが不可欠です。NRMはベンダーフリーの立場から、お客様に最適なツールを選定し、業務改善に資する組み合わせを提案します。効率的な業務遂行を実現するためのシステム構築をサポートいたしますので、ご安心ください。 -
導入メリット
-
専門スタッフが手厚いサポート
NRMの専門スタッフは、幅広い業界経験と専門知識を有しており、お客様の課題に対して的確なアドバイスと解決策を提供します。業務改善プロセス全体を通じて、お客様のビジョンを理解し、効果的なアクションを導きます。お客様との緊密な連携を大切にし、常に最高の結果を追求するために尽力します。

